الفرق بين رياكتنت و كاشف | رياكتانت فس ريجنت
الفرق الرئيسي - التفاعل مقابل الكاشف
يستخدم المصطلحان المتفاعلان والكواشف في التفاعلات الكيميائية العضوية وغير العضوية. على الرغم من أن المصطلحين لهما معاني مماثلة، دورهما في رد فعل معين يختلف عن الآخر. الفرق الرئيسي بين المتفاعلات والكواشف هو أن المتفاعلات هي المركبات التي تستهلك وتشارك مباشرة في التفاعل في حين أن الكواشف تستخدم لقياس مدى تفاعل كيميائي أو لمراقبة التفاعل .
ما هو رد الفعل؟
مفاعل هو مادة التي تشارك مباشرة في تفاعل كيميائي. فإنه يبدأ التفاعل الكيميائي ويستهلك بعد رد فعل. على وجه الخصوص، هناك اثنين أو أكثر من المواد المتفاعلة في تفاعل كيميائي. على الرغم من أن المذيبات تشارك في تفاعل كيميائي، فإنها لا تعتبر متفاعلة. وبالمثل، لا يتم استهلاك المواد الحفازة بعد التفاعل الكيميائي؛ وبالتالي، فإنها لا تعتبر متفاعلة.

ما هو كاشف؟
كاشف في تفاعل كيميائي يسهل التفاعل الكيميائي يحدث، أو أنه يستخدم لكشف وقياس أو دراسة مدى رد الفعل دون أن تستهلك في نهاية التفاعل. ويمكن أن يكون مركب واحد أو خليط من المركبات الكيميائية. دور ونوع الكاشف هي محددة جدا لرد فعل معين. وتستخدم الكواشف المختلفة لردود الفعل المختلفة.
أمثلة على الكواشف المستخدمة بشكل شائع ووظائفها:
كاشف كولين: للتأكسد بشكل انتقائي الكحول الأولي إلى الألدهيد.
كاشف فنتون: لتدمير المركبات العضوية الملوثة.
كاشف غريغنارد: لتجميع مركبات عضوية طويلة السلسلة باستخدام هاليدات ألكيل / أريل.
كاشف نيسلر: لتحديد وجود الأمونيا.
كاشف بينيديكت: للكشف عن وجود خفض السكر (ق). مواد خفض أخرى أيضا إعطاء رد فعل إيجابي.
كاشف فهلينغ: للتمييز بين الكربوهيدرات القابلة للذوبان في الماء والكيتون مجموعات وظيفية.
كاشف ميلون: لتحديد وجود بروتينات قابلة للذوبان.
كاشف تولن: لتحديد وجود مجموعات وظيفية ألدهيد أو ألفا هيدروكسيل كيتون.
يمكن تصنيف هذه الكواشف الكيميائية إلى فئتين؛ الكواشف الكيميائية العضوية والكواشف الكيميائية غير العضوية.
- ديفيسيون كواشف| الكواشف العضوية | الكواشف غير العضوية |
| كاشف كولينز | كاشف نيسلر |
| كاشف فينتون | كاشف بينديكت |
| كاشف غريغنارد | كاشف فهلينغ |
| كاشف ميلون | |
| كاشف تولن |

كاشف كولين
ما هو الفرق بين رياكتنت و كاشف؟
التعريف:
مفاعلات هي المواد التي تبدأ تفاعل كيميائي وتستهلك في هذه العملية.
الكواشف هي المواد التي تسهل التفاعل الكيميائي ولها وظائف محددة.
الاستهلاك في التفاعل الكيميائي:
المواد الفعالة تستهلك في التفاعل الكيميائي؛ فإنها تصبح المنتجات بعد التفاعل الكيميائي.
الكواشف لا تستهلك بالضرورة في تفاعل كيميائي. وهي تستخدم لكشف أو فحص أو مراقبة مدى تفاعل كيميائي أو لتحديد مجموعات وظيفية معينة.
عدد المركبات:
A مفاعل هو مركب واحد.
A كاشف يمكن أن يكون مركب كيميائي واحد أو خليط من عدة مركبات كيميائية.
| كاشف | التركيب |
| كاشف تولن | محلول نترات الفضة (أغنو 3 ) والأمونيا (نه 3 ) |
| > أحجام متساوية من حلول فهلينغ ألف و فهلينغ ل. | فهلينغ's
A A أزرق محلول مائي من النحاس (إي) كبريتات (كسو 4 ) فهلينغ ب هو > طرطرات طرطرات وقلوي قوي (عادة هيدروكسيد الصوديوم) كاشف كولينز |
| مجمع من الكروم (السادس) أكسيد (كرو | 3 ) مع البيريدين في ثنائي كلورو ميثان (تش
2 كل 2 ) كاشف غريغنارد |
| المنتج من تفاعل ألكيل أو هريل أريل مع معدن المغنيسيوم (R-مغ-X) | الضرورة في التفاعلات الكيميائية: |
مفاعلات
تشارك في جميع التفاعلات الكيميائية؛ بل هو عنصر ضروري من التفاعل الكيميائي. يمكن أن يحدث تفاعل حتى بدون مادة كيميائية
كاشف . وبعبارة أخرى، ليست كل التفاعلات الكيميائية بالضرورة تتطلب كاشف كيميائي. إيماج كورتيسي:

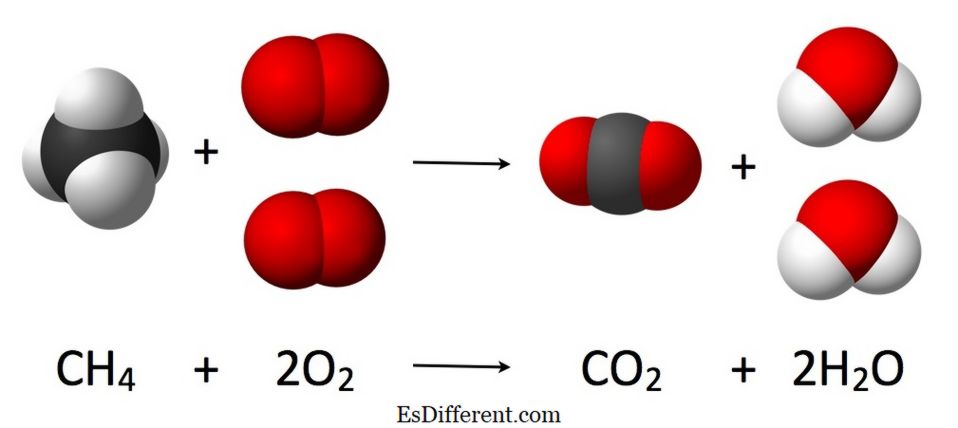
1. "تفاعل احتراق الميثان" بواسطة جينتوروبرت A. روهدجاسك فجينتو [سيسي بي-سا 3. 0] عبر العموم
2. كولينز كاشف من قبل ميفيستو سبا (العمل الخاص) [الملك العام]، عن طريق ويكيمديا كومنز



