الفرق بين هيدروكسيل وهيدروكسيد | هيدروكسيل مقابل هيدروكسيد
فارق الاختلاف - هيدروكسيل مقابل هيدروكسيد
المصطلحان هيدروكسيل وهيدروكسيد الصوت متشابهان جدا لأن كلا منهما له ذرتان مماثلتان، الأكسجين (O = 16) والهيدروجين H = 1). هيدروكسيد هو أيون سلبي مع تهمة واحدة و هيدروكسيل غير موجود في شكله الحر، بل هو جزء من جزيء آخر أو أيون. هيدروكسيد الأيونات هي أكثر تفاعلا من مجموعة الهيدروكسيل في جزيء. هذا هو الفرق الرئيسي بين هيدروكسيل وهيدروكسيد.
ما هو هيدروكسيل؟
هيدروكسيل هو مركب محايد وهو مركب محايد كهربائيا من أيون هيدروكسيد. شكل حر من الهيدروكسيل (• هو) هو جذري وعندما يتم ربط تساهمية لجزيئات أخرى هو ما يسمى مجموعة الهيدروكسيل (-OH). يمكن أن تعمل مجموعات الهيدروكسيل كما نوكليوفيلز ويستخدم هيدروكسيل جذري كحافز في الكيمياء العضوية. مجموعات الهيدروكسيل ليست رد الفعل للغاية كما نوكليوفيلز الأخرى. ومع ذلك، فهي الميسرين في تشكيل قوى قوية داخل الجزيئات تسمى "روابط الهيدروجين".

ما هو هيدروكسيد؟
هيدروكسيد هو أنيون ثنائي الذرات يحتوي على ذرة الأكسجين وذرة الهيدروجين. السندات بين ذرات الأكسجين والهيدروجين تساهمية وصيغتها الكيميائية هي أوه - . التأين الذاتي للمياه تنتج أيونات الهيدروكسيل، وبالتالي أيونات الهيدروكسيل هي جزء طبيعي في الماء. وتستخدم أيونات هيدروكسيد كقاعدة، يجند، نوكليوفيل ومحفز في التفاعلات الكيميائية. وبالإضافة إلى ذلك، تنتج أيونات الهيدروجين الأملاح مع الكاتيونات المعدنية ومعظمهم من فصل في المحاليل المائية، والإفراج عن أيونات هيدروكسيد حلها. العديد من المواد الكيميائية غير العضوية تحتوي على مصطلح "هيدروكسيد" في اسمها، لكنها ليست أيونية وهي مركبات التساهمية التي تحتوي على مجموعات الهيدروكسيل.

ما هو الفرق بين هيدروكسيل وهيدروكسيد؟
هيكل:
هيدروكسيل: هيدروكسيل هو مركب محايد كهربائيا والتي يمكن العثور عليها بطريقتين، كما شكل راديكالي و تساهمية.

هيدروكسيل جذري عندما يكون المستعبدين تساهمية إلى جزيء
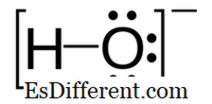
هيدروكسيد: هيدروكسيد هو أيون سالبة الشحنة والشحنة السلبية على ذرة الأكسجين.
هيدروكسيل: توجد مجموعات الهيدروكسيل في العديد من المركبات العضوية. والكحول، والأحماض الكربوكسيلية ومجموعات الهيدروكسيل التي تحتوي على السكر. المركبات التي تحتوي على مجموعات الهيدروكسيل مثل الماء، والكحول، والأحماض الكربوكسيلية يمكن ديبروتوناتد بسهولة.وبالإضافة إلى ذلك، وتشارك هذه المجموعات الهيدروكسيل في تشكيل الروابط الهيدروجين. وتساعد الروابط الهيدروجينية الجزيئات على التمسك معا، وهذا يؤدي إلى امتلاك نقاط غليان وذوبان أعلى. بشكل عام، والمركبات العضوية هي سيئة للذوبان في الماء. تصبح هذه الجزيئات قليلا للذوبان في الماء عندما تحتوي على اثنين أو أكثر من مجموعات الهيدروكسيل.
هيدروكسيد: معظم المواد الكيميائية التي تحتوي على هيدروكسيد تعتبر تآكل جدا، وبعضها ضار جدا. عندما يتم حل هذه المواد الكيميائية في الماء، يعمل أيون هيدروكسيد كقاعدة قوية بشكل لا يصدق. منذ هيدروكسيد ايون يحمل شحنة سالبة، وغالبا ما المستعبدين إلى أيونات موجبة الشحنة.
بعض المركبات الأيونية التي تحتوي على مجموعات هيدروكسيد في جزيءها تذوب جيدا في الماء؛ يمكن أن تؤخذ قواعد تآكل مثل هيدروكسيد الصوديوم (هيدروكسيد الصوديوم) وهيدروكسيد البوتاسيوم (كوه) على سبيل المثال. ومع ذلك، بعض هيدروكسيد الأخرى التي تحتوي على المركبات الأيونية هي غير قابلة للذوبان قليلا في الماء. ومن الأمثلة على ذلك هيدروكسيد النحاس (إي) 2 - اللون الأزرق الساطع] والحديد (إي) هيدروكسيد [في (أوه) 2 - براون].
تفاعلية:
هيدروكسيل : مجموعات الهيدروكسيل أقل تفاعلا بالمقارنة مع مجموعة هيدروكسيد. ولكن، مجموعات الهيدروكسيل تشكل بسهولة روابط الهيدروجين وتساهم في جعل الجزيئات أكثر قابل للذوبان في الماء.
ومع ذلك، فإن الجذور الهيدروكسيلية تفاعلية للغاية ومفيدة جدا في التفاعلات الكيميائية العضوية.
هيدروكسيد: هيدروكسيد (أوه - ) تعتبر المجموعة نوكليوفيل قوي في الكيمياء العضوية.
المراجع: مارتن. شابلن @ btinternet. كوم، M. C. (n. d.). هيدروكسيد الأيونات. استرجاع 28 ديسمبر 2016، من هنا هيدروكسيد أيون: تعريف وصيغة - فيديو ودرس نص. (د.). استرجاع 28 ديسمبر 2016، من هنا هيدروكسيد. (د.). استرجاع 28 ديسمبر 2016، من هنا مجموعة هيدروكسي. (د.). استرجاعها ديسمبر 28، 2016، من هناهيدروكسيل المجموعة: تعريف، هيكل و الفورمولا. (د.). استرجاع 28 ديسمبر 2016، من هنا H. (2014). ما هي مجموعة الهيدروكسيل؟ ريتريفد ديسمبر 28، 2016، فروم هير

