الفرق بين ليسين و L-ليسين | ليسين مقابل L-ليسين
الفرق الرئيسي - ليسين مقابل L-ليسين
ليسين و L- ليسين كلاهما نوع من الأحماض الأمينية، وتقاسم نفس الخصائص الفيزيائية على الرغم من أن هناك بعض الفرق بينهما. و الفرق الرئيسي بين ليسين و L- يسين هو في القدرة على تدوير ضوء مستقطب الطائرة. ليسين هي نشطة بيولوجيا حمض α- أمينو الأساسية التي تحدث بشكل طبيعي. ويمكن أن يحدث في شكلين إسوميريك نظرا لإمكانية تشكيل اثنين من إنانتيوميرس مختلفة حول ذرة الكربون مراوان. وتعرف هذه النماذج بأشكال L- و D-، على غرار التشكيلات اليسرى واليد اليمنى. ويقال أن هذه L- و D- أشكال لتكون نشطة بصريا وتناوب ضوء المستقطب الطائرة بمعنى مختلف. في اتجاه عقارب الساعة أو عكس اتجاه عقارب الساعة. إذا كان ضوء تدور يسين عكس اتجاه عقارب الساعة، ثم المعارض الخفيفة ليفوروتاتيون، وكما هو معروف L- يسين. ومع ذلك، ينبغي أن نلاحظ بعناية هنا أن العلامات D- و L- من الأيزومرات ليست هي نفسها كما في وضع العلامات و- ل.
ما هو ليسين؟
ليسين هو الأحماض الأمينية الأساسية وهو لا توليفها في الجسم ويجب أن يتم توفيرها من قبل النظام الغذائي العادية. ولذلك، ليسين هو حمض أميني أساسي للبشر. وهو مركب عضوي مهم بيولوجيا يتكون من أمين (-NH 2 ) ومجموعة وظيفية كربوكسيلية (كوه) مع الصيغة الكيميائية نه 2 - (تش 2) 4 -CH (NH 2 ) - COOH. والعناصر الرئيسية لليسين هي الكربون والهيدروجين والأكسجين والنيتروجين. وفي الكيمياء الحيوية، تعرف الأحماض الأمينية التي تحتوي على كل من الأمين ومجموعات حمض الكربوكسيل الملتصقة بأول ذرة كربون ألفا < α-أمينو أسيدس . وهكذا يعتبر ليسين أيضا الأحماض الأمينية α. ويرد هيكل يسين في الشكل 1.
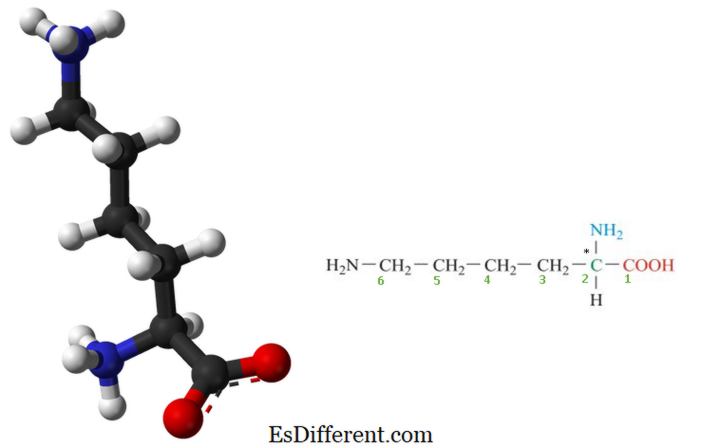
ليسين أساسي في الطبيعة لأنه يحتوي على اثنين من الأمينية الأساسية مجموعات وحمض واحد مجموعة حمض الكربوكسيلية. وبالتالي، فإنه يشكل أيضا رابطة الهيدروجين واسعة النطاق بسبب وجود مجموعتين أمينية.
مصادر جيدة من الليسين هي مصادر البروتين الحيواني مثل البيض واللحوم الحمراء والضأن والخنزير والدواجن والجبن وبعض الأسماك (مثل سمك القد والسردين). ليسين أيضا غنية بالبروتينات النباتية مثل فول الصويا والفول والبازلاء. ومع ذلك، فإنه هو الحد من الأحماض الأمينية في معظم الحبوب الحبوب ولكن وفيرة في معظم البقول والبقوليات.
ليسين لديها أربع مجموعات مختلفة حول 2
ند الكربون، و هيكل غير المتماثلة .أيضا، ليسين هو حمض أميني نشط بصريا بسبب وجود هذه ذرة الكربون غير المتماثلة أو مراوان. وهكذا، يسين يمكن أن يخلق ستيريويسوميرس التي هي جزيئات إيزومرية لها نفس الصيغة الجزيئية، ولكن تختلف في توجهات ثلاثية الأبعاد من ذراتها في الفضاء. إنانتيوميرس هي اثنين من ستيريويسوميرس التي ترتبط بعضها البعض من قبل انعكاس أو أنها صور مرآة من بعضها البعض التي لا يمكن فرضه. ليسين متاح في شكلين إنانتيوميريك المعروفة باسم L- و D- و إنانتيوميرس من ليسين وتعطى في الشكل 2. الشكل 2: إنانتيوميرس من حمض أميني ليسين. يتم ترتيب مجموعات كوه، H، R و NH2 حول ذرة C في اتجاه عقارب الساعة، ويسمى إنانتيومر L- شكل و D- شكل خلاف ذلك. L- و D- تشير فقط إلى الترتيب المكاني حول ذرة الكربون ولا تشير إلى النشاط البصري. في حين أن أشكال L- و D- من جزيء مراوان تفعل تدوير طائرة من الضوء المستقطب في اتجاهات مختلفة، بعض أشكال L- أو (أشكال D) تدوير الضوء إلى اليسار (ليفو أو L- شكل) والبعض إلى اليمين (دكسترو أو د). ل- و د- أشكال تسمى الأيزومرات الضوئية.

L- ليسين و D- ليسين هي إنانتيوميرس من بعضها البعض لها نفس الخصائص الفيزيائية، باستثناء الاتجاه الذي يدورون ضوء الاستقطاب. لديهم غير قابلة للتراكب علاقة صورة مرآة. ومع ذلك، فإن تسميات D و L ليست شائعة في الأحماض الأمينية بما في ذلك ليسين. وهي تدور الضوء المستقطب من الطائرة بنفس الحجم ولكن في اتجاهات مختلفة. ويسمى D و L-إيسومر من يسين الذي يدور الضوء المستقطب الطائرة في اتجاه عقارب الساعة كما ديكستروروتاتوري أو
د-يسين وتلك التي تدور الضوء المستقطب الطائرة في اتجاه عقارب الساعة يسمى كما ليفوروتاتوري أو L-ليسين (الشكل 2). L- ليسين هو
الأكثر استقرارا شكل مستقر من يسين . D- يسين هو شكل اصطناعي من يسين ويمكن توليفها من l- يسين عن طريق الترسيم. يتم استخدامه في تجهيز بولي-د- يسين، والذي يستخدم كمواد طلاء لتعزيز مرفق الخلية. L- ليسين يلعب دورا هاما في جسم الإنسان، في امتصاص الكالسيوم، وتطوير البروتين العضلي، وتوليف الهرمونات والأنزيمات، والأجسام المضادة. إندستريالي، L-ليسين يتم إنتاجها بواسطة عملية التخمير الميكروبية باستخدام كورينيباكتريوم غلوتاميكوم. ما هو الفرق بين ليسين و L- يسين؟
ليسين و L- ليسين لها نفس الخصائص الفيزيائية، باستثناء الاتجاه الذي يدورون الضوء المستقطب. ونتيجة لذلك، L-ليسين قد يكون لها تأثيرات بيولوجية مختلفة وخصائص وظيفية مختلفة. ومع ذلك، فقد أجريت بحوث محدودة جدا من أجل التمييز بين هذه الآثار البيولوجية والخصائص الوظيفية. بعض هذه الاختلافات قد تشمل،
طعم
L-ليسين:
L- أشكال الأحماض الأمينية تميل إلى أن تكون لا طعم له. D-ليسين:
D- أشكال الأحماض الأمينية تميل إلى الذوق الحلو. لذلك l- ليسين قد يكون أقل / لا أحلى من ليسين.
وفرة
L-ليسين:
و l- أشكال الأحماض الأمينية بما في ذلك l- ليسين هو الشكل الأكثر وفرة في الطبيعة.وكمثال على ذلك، تسعة من تسعة عشر الأحماض الأمينية L وجدت عادة في البروتينات ديكستروروتاتوري والباقي هي ليفوروتاتوري. D-ليسين:
وقد وجد أن أشكال الأحماض الأمينية التي تمت ملاحظتها تجريبيا نادرا جدا. المراجع: سولومونز، T. W. غراهام، أند غريغ B. فريهل (2004). الكيمياء العضوية (8
ث إد). هوبوكين: جون وايلي & سونس، Inc. إيفرهاردوس، A. (1984). ستيريوشيميستري، أساس ل هراء متطور في الدوائية و الصيدلة السريرية، المجلة الأوروبية لعلم الصيدلة السريرية، 26 ، 663-668. إيماج كورتيسي: "L-ليسين-مونوكاتيون-فروم هيدروكلوريد-ديهيدريت-شتال-3D-بالز" بواسطة بن ميلز - عملك الخاص عبر ويكيميديا كومنز


