الفرق بين الكانكين والكن | ألكانيس فس ألكين
الفرق الرئيسي الكانكس مقابل الكينيس
الكانك والكنيس نوعان من الأسر الهيدروكربونية التي تحتوي على الكربون والهيدروجين في هيكلها الجزيئي. والفرق الرئيسي بين الكانكين والكنيس هو تركيبهما الكيميائي؛ الألكانات هي هيدروكربونات مشبعة مع الصيغة الجزيئية العامة ل n H 2n + 2 و ألكينس يقال إنها مجموعة هيدروكربونية غير مشبعة لأنها تحتوي على رابطة مزدوجة بين كربون الذرات. لديهم الصيغة الجزيئية العامة ل n H 2n.
ما هي "الكانانات"؟
تحتوي الألكانات على روابط واحدة فقط بين ذرات الكربون والهيدروجين (السندات C-C و C-H السندات). ولذلك، تسمى "الهيدروكربونات المشبعة". وطبقا لنموذج التهجين المداري، فإن جميع ذرات الكربون في ألكينس لها التهجين <سب> 3 . أنها تشكل روابط سيغما مع ذرات الهيدروجين، والجزيء الناتج له هندسة رباعي رباعي. ويمكن تقسيم الألكانات إلى مجموعتين وفقا لترتيباتها الجزيئية؛ ألكانيس أسيليك (C n H 2n. +2 ) و ألكانيس دوري (C n H 2n ).

ألكنس هي الهيدروكربونات، التي تحتوي على الكربون الكربون (C = C) الرابطة المزدوجة.
"أوليفينز" هو الاسم القديم المستخدم للإشارة إلى عائلة ألكين. أصغر عضو في هذه العائلة هو الإيثان (2 H 4 )؛ كان يطلق عليه أوليفيان t غاس (باللاتينية: ' أوليم' تعني 'أويل' + 'فاكير' تعني 'جعل') في الأيام الأولى. ويرجع ذلك إلى أن التفاعل بين C 2 H 4 والكلور يعطي C 2 H 2 كل 2 نفط.

التركيب الكيميائي للألكان والكنز
الكانكات:
الكانكس لها الصيغة الجزيئية العامة n H 2n + 2. الميثان (تش 4 ) هو أصغر ألكان. - ديف المادة قبل منتصف الجدول>>
الاسم| الصيغة الكيميائية | هيكل أسيليك | الميثان |
| تش | 4 تش | 4 الإيثان < > C |
| 2 | H 6 CH 3 | CH 3 البروبان C |
| 3 | H 8 CH 3 | CH 2 CH 3 البوتان C |
| 4 | H 10 CH 3 CH | 2 CH 2 CH 3 البنتان C 5 |
| H | 12 CH 3 CH | 2 CH 2 CH 2 CH 3 الهكسين C 6 H |
| 14 | CH 3 CH 2 | CH 2 CH 2 CH 2 CH 3 الهيبتان C 7 H |
| 16 | CH 3 CH 2 | CH 2 CH 2 CH 2 CH 2 CH 3 أوكتان C 8 H 18 |
| CH | 3 CH 3 CH | 2 CH 2 CH 2 CH 2 تش 3 تش 3 ألكنس: ألكنس لها الصيغة الكيميائية العامة < n H 2n .وتعتبر الألكنيز هيدروكربونات غير مشبعة لأنها لا تحتوي على العدد الأقصى من ذرات الهيدروجين التي يمكن أن تكون مملوكة لجزيء هيدروكربوني. |
الاسم الصيغة الكيميائية بنية إيثين 2
| H | 4 | تش |
| 2 = | تش 2 بروبلين | 3 H 6 تش |
| 3 | تش 3 H | 8 H 8 تش |
| 2 < | تش 2 تش 3، | تش 3 تش = تشش < > 3 بينتين C 5 H 10 CH 2 = |
| CHCH | 2 CH 2 تش | 3، تش 3 تش <3 تش <تشش 2 تش 3 هيكسين < > 12 CH 2 = CHCH 2 CH |
| 2 | CH 2 CH 3 | CH 3 CH = CHCH 2 CH 2 CH 3 CH 3 CH 2 CH = CHCH 2 CH 3
Heptene C 7 H 14 CH = CHCH < 2 CH 2 |
| CH | 2 CH 2 CH | 3 CH 3 CH = CH < 2 تش 2 تش 2 تش 2 تش 2 تش < >: تفاعلية: الألكانات خاملة لكثير من الكواشف الكيميائية. وذلك لأن الكربون الكربون (C-C) والكربون - الهيدروجين (C-H) السندات قوية جدا منذ ذرات الكربون والهيدروجين لديها تقريبا نفس القيم الكهربية. ولذلك، فمن الصعب جدا لكسر سنداتها، إلا إذا كانت ساخنة إلى درجات حرارة عالية إلى حد ما. الاحتراق: يمكن أن يحرق الألكان بسهولة في الهواء. ويسمى التفاعل بين الألكانيس والأكسجين الزائد "الاحتراق". في هذا التفاعل، تتحول الألكانات إلى ثاني أكسيد الكربون (كو 2 ) والماء. h n h 2 |
+ (n + n / 2) o
2 < 2
4
4 h 10
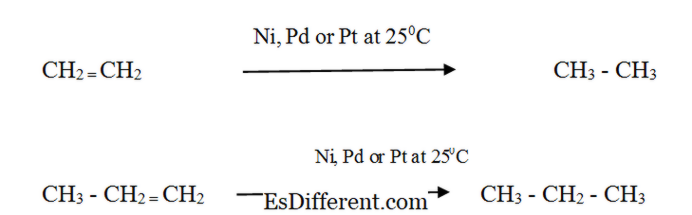
+ 13/2 س 2 → 4 كو 2 + 5 h < > 2 O البوتان الأكسجين ثاني أكسيد الكربون المياه ردود الفعل الاحتراق هي ردود فعل طاردة للحرارة (أنها تعطي الحرارة). ونتيجة لذلك، تستخدم الألكانات كمصدر للطاقة. ألكنيس: تفاعلية: تتفاعل ألكينز مع الهيدروجين في وجود حفاز معدني مقسم بشكل دقيق لتشكيل الكان المقابل. معدل التفاعل منخفض جدا بدون عامل حفاز.
يستخدم الهدرجة التحفيزية في صناعة الأغذية لتحويل الزيوت النباتية السائلة إلى الدهون شبه الصلبة في صنع السمن والصلب الطهي الدهون. الخواص الفيزيائية للكنس والكنيس النماذج الكانكس: الكانكس موجودة كغازات و سوائل و مواد صلبة. الميثان والإيثان والبروبان والبيوتان هي غازات في درجة حرارة الغرفة. الهياكل غير المقشورة للهكسان والبنتان والهبتان هي سوائل. الألكانات التي لها وزن جزيئي أعلى هي المواد الصلبة. تش 4 إلى الصفحة السابقة 4 H 10
هي الغازات
17
H
36
هي سوائل و
ألكانات ذات وزن جزيئي أعلى هي مواد صلبة ناعمة
ألكنيس:
تظهر ألكنس خصائص مادية مماثلة للألكان المقابل. ألكنس ذات الأوزان الجزيئية المنخفضة (<2 H
4 توك 4 H 8 ) هي غازات في درجة حرارة الغرفة والضغط الجوي.ألكنس وجود وزن الجزيئي العالي هي المواد الصلبة. الذوبان:
الألكانيس: الألكانات لا تذوب في الماء. يتم حلها في المذيبات العضوية غير القطبية أو ضعيفة القطبية. ألكنيس: ألكنس جزيئات قطبية نسبيا بسبب C = C السندات. وبالتالي، فهي قابلة للذوبان في المذيبات غير القطبية أو المذيبات من قطبية منخفضة. الماء هو جزيء قطبي و ألكينس قابلة للذوبان في الماء قليلا. الكثافة: الألكانات: كثافة الألكانات أقل من كثافة المياه. وتبلغ قوتها حوالي 0. 7 غل -1 ، معتبرة كثافة الماء كما 1. 0 g مل
-1
. ألكنيس: كثافة ألكنس أقل من كثافة المياه. نقاط الغليان: ألكانيس: تزداد نقطة الغليان من الألكانات غير المقشورة بشكل سلس مع تزايد عدد ذرات الكربون والوزن الجزيئي. بشكل عام، الألكانات متفرعة لديها نقاط الغليان أقل بالمقارنة مع ألكانات غير مقروء، وجود نفس العدد من ذرات الكربون. ألكنيس : نقاط الغليان مماثلة للألكانات المقابلة مع اختلاف بسيط. المراجع: كليفسنوتس. (د.). استرجاع 06 يوليو 2016، من هنا.
الخواص الفيزيائية للكنس. (2013). ريتريفد جولاي 06، 2016، من هنا
زوم ديركتوري-مودوس. (د.). ريتريفد جولاي 06، 2016، من هنا الخصائص الكيميائية للألكانات: ويزنوتس. com- مجانا غسس و سكك: دروس، ورقات الماضي ومسابقات. (د.). ريتريفد جولاي 06، 2016، من هنا
قطبية. (د.). ريتريفد جولاي 06، 2016، من هنا ثنائي القطب لحظات. (2013). ريتريفد جولاي 06، 2016، من هنا
إسومر الهيكلي. (د.). ريتريفد جولاي 06، 2016، من هنا
مقدمة إلى ألكينس. (د.). ريتريفد جولاي 06، 2016، فروم هير إيماج كورتيسي: "ألكين نامس" بقلم كريس إيفانز - (CC0) عبر كومونس ويكيميديا "هيدروكربونات C4 مشبعة بالألوان" بواسطة ففاسكونسيلوس - بوبليك دومين) عبر كومونس ويكيميديا




